EGT-Wärmetechnik (Wärmebedarf)
[TEC/GM]
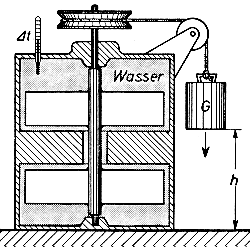
Die Joulesche Wärmemenge

1840 ermitelte er die Temperaturerhöhung in einem Rührbehälter (siehe Bild rechts), die ein fallendes Gewicht erzeugte, wenn es im Fallen das Wasser mit Schaufelrädern umrührte. Er fand heraus, dass ein Gewicht von 772 Pfund, das einen Fuß fällt die Temperatur von einem Pfund Wasser um 1°F erhöht. Das ergibt für die Wärmemenge von 1 cal die heutige Entsprechung von 4,15 J.
Seine Experimente haben gezeigt, dass Wärme durch Bewegung erzeugt wird und haben damit die Grundlage für die Theorie der Wärmelehre mit dem heute anerkannten Wärmeäquivalent von 1 cal = 4,184 J gelegt.
- der Masse des zu erwärmenden Stoffes ...m
- sowie dessen spezifischer Wärme ...c
- und seiner Temperaturänderung ......Δϑ
Q = m * c * Δϑ
Beispiel
Zwei Liter Wasser sollen von 20 Grad auf 80 Grad erwärmt werden. Welche Wärme ist dafür nötig?Lösung: Die Menge Wasser kann direkt als Gewicht angegeben werden, da 2 Liter Wasser einer Masse von 2kg entsprechen, damit ist m = 2kg. Die spezifische Wärmekapazität von Wasser entnimmt man einer Tabelle und beträgt c = 4190J · kg-1K-1. Die Temperaturdifferenz beträgt 60 Grad Celsius, was auch 60 Kelvin entspricht.
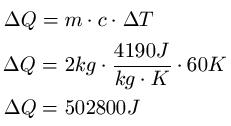
Berechnung des Wärmebedarfs
Heißwassererzeugung
Die Joulesche Wärmemenge ist der Wärmebedarf für die Warmwasserezeugung.
Die Elektrowärme entspricht der Elektrischen Arbeit W an einem Ohmschen Widerstand.
W = I2 * R * t
Aus der Stromwärme wird das Wasser erwärmt, wobei ev. Verluste berücksichtigt werden müssen.
Q = W * η
Für die elektrische Energie in Wattstunden [Wh] ergibt sich die Beziehung: \( W = \frac{ m \cdot c \cdot \Delta {ϑ} }{ 3600 \cdot \eta } \)
m ... Masse in kg
c ... Spezifischer Wärmekapazität in J/kgK
Δϑ ... seiner Temperaturänderung in K
η ... dem Wirkungsgrad
3600 ... Umrechnungsfaktor von Sekunden in Stunden
Raumheizung
Der Wärmebedarf für einen Raum steht für die Wärmeverluste in diesem Raum und ist ausschlaggebend für die Dimensionierung einer Heizung.
Den Wärmestrom durch die einzelnen Flächen erhält man, indem man den U-Wert mit der Fläche in m² und der Temperaturdifferenz multipliziert.
P = U-Wert * Fläche * Δϑ
Damit erhält man für ein Δϑ von 30K etwa folgende Transmissionswärmeverluste:
 home
home